三家医院三种结果,患者的CA125水平究竟是多少?
2023-06-06 15:17 文章来源:
作者:江跃红[1] 姜廷军[1] 李莹[2]
单位:[1]哈尔滨医科大学附属第四医院检验科 [2]深圳迈瑞生物医疗电子股份有限公司
血清糖类抗原CA125是最常用的卵巢癌标志物,尤其是浆液性癌的首选肿瘤标志物。CA125阳性率与肿瘤分期、组织学类型有关,晚期、浆液性癌患者的阳性率(约84.1%~92.4%)显著高于早期卵巢癌(约43.5%~65.7%)及非浆液性癌患者的阳性率。
有研究发现,CA125在绝经后人群的应用价值更高。在绝经后人群中,CA125诊断卵巢癌的敏感性(79.1%~90.7%)和特异性(79.1%~89.8%)均优于绝经前人群(敏感性 69.8%~87.5%,特异性 63.3%~85.7%)。外科手术或化疗后,87%~94%的卵巢癌病例中,血CA125浓度与疾病进程相关性较好,可提示肿瘤的进展或消退。有研究认为,满意减瘤术后,7天内CA125可下降到最初水平的75%以下[1]。
今天分享一例“CA125在卵巢源性腹膜癌术后复发监测上的应用案例”,探讨肿瘤标志物使用的注意事项。
案例背景
2022年1月26日,科室接到患者投诉,称我院CA125检测结果不准。经详细沟通,了解到该患者一直在我院监测CEA、CA125,且CA125在2021年下半年监测过程中呈逐渐升高趋势,2021年12月24日测值为67.38U/mL。
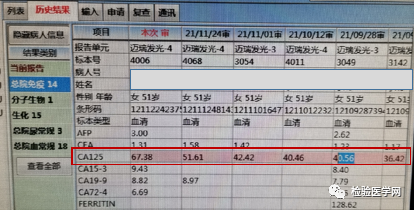
2022年1月,患者在当地肿瘤医院检测CA125,测值为38U/mL;又前往当地另一家医院检测,其CA125测值为29U/mL。因此,患者质疑我院测值不准。
排查分析过程
患者,女,51岁,2021年9月~2021年12月随访过程中,CEA结果无显著波动、呈阴性。CA125从2021年9月开始持续升高,至12月24日升高至67.38U/mL。故临床做复发处理,建议患者做进一步相关检查。
进一步了解到患者复查的两家医院使用的CA125检测系统非我院所用的国产M品牌检测系统。
我们先进行了检测系统排查,样本测试当天该项目质控在控,仪器无异常报警,当天其余样本测试结果均无异常。可初步排除检测系统问题。患者处于绝经期,排除经期所致的CA125结果升高。
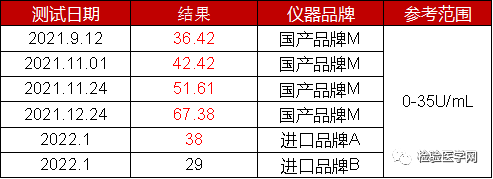
是否样本存在其他干扰因素?与患者沟通,次日重新采血检测。次日,将同一管血分为4份,在2h内送往多家医院进行CA125测试。结果如下。

结果显示,同一样本各检测系统结果均为阳性,但系统间存在测值偏差。
因肿瘤标志物的国际标准化尚未完善,根据国际标准化组织 ISO 17511“校准物质和质控物质定值的计量学溯源性”的分类,CA125既无国际标准物质,也无国际参考测量程序。加上不同厂家的试剂采用不同的抗体标记(抗体异质性)、不同的定标品、分析仪器特性差异等,不同厂家的检测结果不可互换。因此,指南建议同一患者在治疗前后及随访中,应尽可能采用同一种方法和试剂。在患者监测中,若更改肿瘤标志物的检测方法,应重新设定患者的基线水平[2]。
因此,该患者进行CA125监测,其测值持续升高的趋势较具体检测数值更值得关注。加做HE4等项目,结果显示CA72-4及HE4呈阳性。
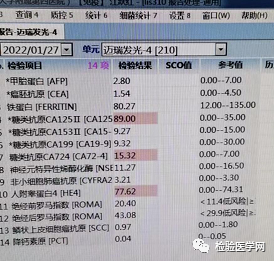
同管血结果比对消除了患者关于检测结果准确性的疑虑后,我们再来结合患者的临床信息,梳理CA125的变化趋势。监测期间,CA125测值变化趋势曲线图如下所示。
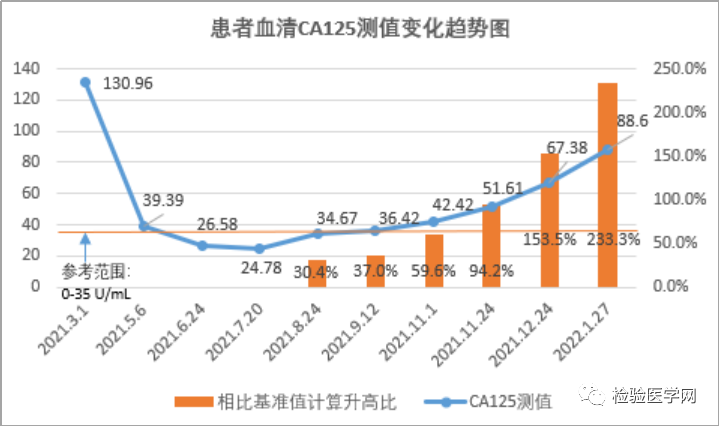
从临床了解到,该患者曾被确诊为卵巢源性腹膜癌,2019年12月在我院放射治疗,后定期复查CA125。2021年3月,CA125结果突然升高至130.96U/mL,但影像检查显示情况稳定。临床采用单药化疗加靶向治疗的方式,3月至5月期间进行4次治疗,结果降至正常范围以内,最低点为2021年7月20日测值24.78U/mL。在定期随访监测过程中,2021年9月结果超过正常参考区间,且呈持续升高趋势。
目前各指南对于CA125用于化疗疗效监测已有定论,但对于如何定义最佳的化疗有效应答尚未达成共识[3],现有对化疗有效的定义为:CA125的水平较治疗前下降大于50%,且维持至少28天[4]。该定义系统适用的情况为治疗前的标本检测值至少超过正常参考范围上限的2倍。
国际妇科肿瘤协作小组(Gynecologic Cancer Intergroup,GCIG)提出连续性监测CA125,以下检测结果提示肿瘤进展:对于术前CA125水平处于正常参考范围的患者,术后2次CA125水平超过参考范围上限的2倍;对于术前即有CA125升高的患者,术后2次检测CA125水平超过其自身最低值(2次检测要求间隔1周进行)。
根据《肿瘤标志物的临床应用建议》中肿瘤标志物的随访原则,随访中如发现肿瘤标志物测值明显升高(高出首次随访值25%),应在1个月内复测1次,连续2次升高可预示复发或转移[2]。
综合以上各指南关于CA125测值变化对肿瘤复发的提示,将2021年6月24日测值26.58U/mL作为化疗后监测基础值。2021年9月,监测指标已呈阳性,且升高幅度37%,超过25%。因此临床基于9月的结果已可提示患者存在复发风险,因患者后续转院治疗,2022年3月联系到患者,确认体内肿瘤复发属实,并已于当地肿瘤医院进行治疗。
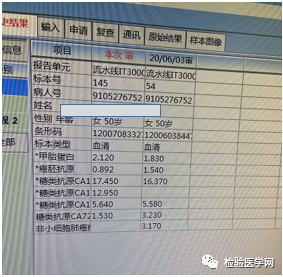
因本院化学发光检测系统切换成国产品牌M之前,一直使用进口品牌A。从Lis系统查询到,该患者品牌A首次监测CA125为2020年6月3日,测值16.37U/mL,直至2022年1月其检测结果才略超过参考范围(38U/mL)。因此,如果使用品牌A进行监测,临床给予肿瘤复发提示的时间节点,相较国产品牌M检测系统,会晚4个月左右。
案例总结
肿瘤标志物可应用于高危人群筛查、肿瘤患者预后评估、疗效监测、复发预测等场景。
在肿瘤疗效监测、复发监测应用场景中,指南建议同一患者在治疗前后及随访中,应尽可能采用同一种方法和试剂。在结果判读方面,当患者术后标志物水平已降至参考范围以内,在持续监测过程中,若肿瘤标志物结果仍为阴性,即使其数值存在升高趋势,可能并不易引起患者及临床关注。往往只有在检测结果转为阳性后,我们才开始关注其升高幅度,如本文案例所示。
因此对于同一患者血清肿瘤标志物的持续监测,若监测数值变化能更早地提示阳性结果,更利于临床对患者体内的肿瘤复发做出更早的预判,从而采取相应的治疗措施。
【参考文献】
[1] 卵巢癌诊疗指南(2022版)
[2] 中华医学会检验分会,卫生部临检中心,中华检验医学杂志编辑委员会,肿瘤标志物的临床应用建议.中华检验医学杂志2012年2月第35卷第2期
[3] Gronlund B, Høgdall C. Should CA-125 response criteria be preferred to response evaluation criteria in solid tumors (RECIST) for prognostication during second-line chemotherapy of ovarian carcinoma? J Clin Oncol. 2004 Oct 15;22(20):4051-8.
